|
|
免疫功能正常的人感染刚地弓形虫(简称弓形虫)后通常是无症状的,但免疫功能低下者感染可能出现严重的临床症状,甚至导致致命的后果。由于器官移植者实体移植器官的多样性、免疫抑制程度的差异性以及弓形虫病发病率相对较低等特点,临床上对器官移植受者弓形虫感染的风险认识不足。因此,本文就实体器官移植受者弓形虫病的临床表现、发病机制、诊断、预防和治疗作一综述,旨在为临床上实体器官移植后的弓形虫病诊治提供参考。
实体器官移植与弓形虫病
作者:黄子芸1、吕芳丽1,2,3
作者单位:1.中山大学中山医学院寄生虫学教研室、2.中山大学热带病防治研究教育部重点实验室、3.广东省媒介生物防控工程技术研究中心
刚地弓形虫(Toxoplasma gondii)(简称弓形虫)是一种专性细胞内寄生原虫,全世界约有超过30%的人被感染。弓形虫病患病率和临床表现的严重程度可因地理区域而异。人因食入含有弓形虫包囊的未煮熟的肉、摄入被猫粪便中卵囊污染的食物而感染。此外,人也可以通过器官移植和输血感染弓形虫(但通过输血传播弓形虫的情况较为少见)。
在中间宿主包括人体内,弓形虫滋养体在细胞内繁殖并通过血液播散到身体的各个部位,如中枢神经系统、肺、骨骼肌、心脏和胎盘等。原发性急性弓形虫感染后,宿主的免疫系统可抑制滋养体的繁殖,使其形成包囊,包囊可在宿主组织中终生存在。免疫功能正常的人感染弓形虫后多呈无症状的带虫状态,仅少数感染者出现流感样综合征,伴有发热和淋巴结肿大等。免疫功能低下或免疫功能受抑制的患者感染弓形虫后可引起严重的后果,导致弓形虫脑炎、弓形虫心肌炎、弓形虫肺炎、弓形虫视网膜脉络膜炎和全身淋巴结炎。
实体器官移植(SOT)受者因需要长期使用免疫抑制剂治疗而被视为弓形虫病的高危人群。SOT后的弓形虫病可由免疫抑制导致受者体内隐性弓形虫感染的活化、从携带弓形虫包囊的供体移植器官中获得原发性感染或食用被弓形虫卵囊污染的食物等所引起。由于SOT后的弓形虫病病例数相对较少,临床表现多样,且有关信息缺乏,导致临床上对其缺乏明确的或达成共识的治疗方案。
本文通过检索1980~2020年Pub Med和中国知网上SOT后的弓形虫病相关文献,综述了受者在心脏、肝脏和肾脏移植后出现弓形虫病的发病机制、诊断、预防和治疗方案,供相关研究者和医务工作者参考。
1 SOT后的弓形虫病的临床表现和发病机制
由于SOT前、后免疫抑制药物的使用,可导致受者的CD4+T细胞水平降低,引发弓形虫病。SOT引起的弓形虫感染主要见于以下几种情形:由血清抗弓形虫抗体阳性的供体(D+)传染给血清抗弓形虫抗体阴性的受者(R-)(即供体/受者为D+/R-),或由血清抗弓形虫抗体阳性受者(即R+)移植前隐性弓形虫感染的活化,或由D+传染给R+(即供体/受者为D+/R+)。
本文对1980~2020年Pub Med和中国知网上101例SOT后的弓形虫病病例统计结果显示,心脏移植后的弓形虫病占41.58%(42/101)、肾移植后的占31.68%(32/101)、肝移植后的占19.8%(20/101)、多器官移植后的占4.95%(5/101)、胰腺移植后的占0.99%(1/101)、小肠移植后的占0.99%(1/101)。由于弓形虫感染好发于心肌,因此心脏移植者的弓形虫病比其他器官移植者的发病率高。Campbell等的统计结果显示,心脏移植以外的病例数以肾移植者为最多,其次是肝脏移植者。多器官移植如肝-肾-胰腺移植、肝-肾移植、肾-胰腺移植等引起的弓形虫病仅有数例,胰腺和小肠移植引起的弓形虫病各有1例。
本文对报道病例数最多的3类SOT(包括心脏、肝脏和肾脏)后的弓形虫病的临床症状和发病机制进行分析,病例资料详见表1。
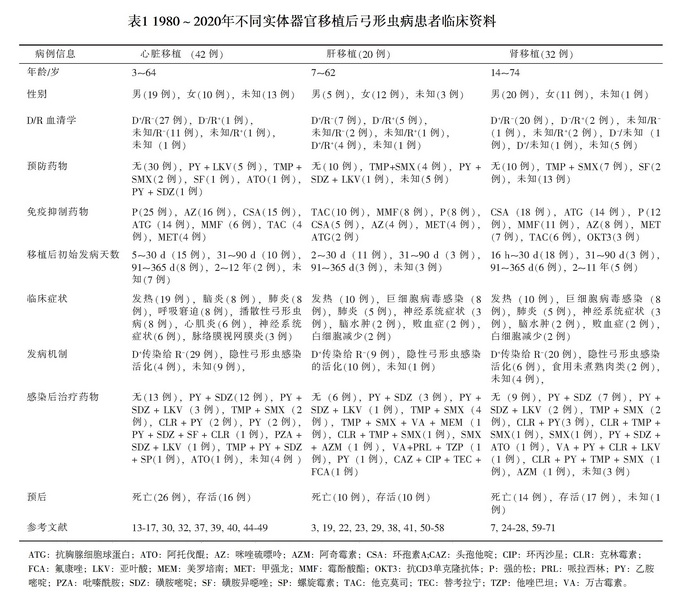
1.1 心脏移植后的弓形虫病
弓形虫的包囊通常寄生于骨骼肌和心肌,因而心脏移植受者弓形虫感染的风险较高。西班牙多中心的一项研究数据显示,SOT受者弓形虫病的发病率为0.14%,其中心脏移植受者的发病率最高,为0.6%。西班牙一医疗机构中315例心脏移植受者的弓形虫病发病率为0.6%(2/315)。美国斯坦福大学医学中心1980~1996年的研究资料显示,在620例心脏移植受者中,98例术前R+(包括D-/R+组和D+/R+组)在移植术后均未出现弓形虫感染活化的临床症状,但在D+/R-组观察到4例移植后感染弓形虫的病例,且这4例受者最终均死于弓形虫病。另一项研究显示,4例R-在接受D+心脏移植后(D+/R-),2例出现弓形虫病;16例R+在接受心脏移植后(包括D+/R+组和D-/R+组)无1例患弓形虫病。上述资料表明,心脏移植前R-在移植后的弓形虫感染大多来源于D+。
与隐性弓形虫感染的活化相比,心脏移植出现的弓形虫感染以急性弓形虫病多见,临床症状通常出现在移植术后的前3个月,最常见的为弓形虫脑炎、发热性弓形虫心肌炎、弓形虫肺炎或累及多器官的播散性弓形虫病。
心脏移植后R+隐性弓形虫感染活化的病例极少,且无明显的临床症状,可能与受者体内有一定的保护性免疫力有关。Castagnini等报道1例58岁女性糖尿病患者因缺血性心肌病接受心脏移植的病例,受者移植前血清抗弓形虫IgG阳性(IgG+)、IgM阴性(IgM-),接受D+的心脏移植后,未采取抗弓形虫预防措施。在术后的5次检查中,受者的抗弓形虫抗体与移植前的检查结果相同(IgG+、IgM-);组织学检查也未发现弓形虫感染的复发;临床表现仅见发热。心肌内膜活检结果提示受者发生3级急性排斥反应,并伴有心血管炎症状,受者在移植后第41天死亡。尸检组织学观察发现,受者存在心脏肥大、弓形虫肺炎和弓形虫脑炎。推测可能是由于受者手术中大量出血,手术期间和术后多次接受输血,导致其血液稀释,间接影响了血清学检查的灵敏度;另外,弓形虫也可能通过供体的心脏或血液传染给受者,或是由受者体内隐性弓形虫感染的活化所致。因此R+在心脏移植术后应注意隐性弓形虫感染复发的可能。
1.2 肝移植后的弓形虫病
Antony于1972年首次报道了肝移植相关的弓形虫病。
Barcán等的研究显示,在2002年以前只有7例肝移植后弓形虫病确诊病例报道,其中2例为弓形虫原发性感染,3例为移植前隐性弓形虫感染的活化,2例发病机制不明。
Barcán等报道了1例D-/R+肝移植后第41天隐性弓形虫感染活化引起的肺炎病例,该病例虽然接受过预防性治疗,但并未完全阻止弓形虫病的发展。
Fernàndez-Sabé等报道了2000~2009年11家医院的多中心研究,结果显示15800例SOT受者中有22例出现弓形虫病(0.14%),其中心脏移植者12例、肾脏移植者6例、肝脏移植者4例。
Fabiani等对1998~2018年SOT后出现的寄生虫感染(包括非肠道原虫、肠道原虫、肠道蠕虫和非肠道蠕虫感染)的分析结果显示,肝移植后的弓形虫病占所有移植后弓形虫病病例的11.7%(19/162)。
有文献报道,1972~2016年,R-在移植D+的肝后,确诊为弓形虫病的病例数量占肝移植后弓形虫病总病例数的30%(10/31)。
Galván等报道4例R+从D-获得肝移植后(D-/R+),3例肝内的弓形虫包囊活化,出现临床并发症而死亡;同时还观察到所有R+在接受D+的肝移植后(D+/R+),受者体内的隐性弓形虫感染活化,PCR检测出弓形虫特异性基因,且血清抗弓形虫IgG和IgM的水平较移植前升高。
此外,孙雁等报道1例移植术前血清抗弓形虫IgM+受者在移植D-的肝脏后,出现发热和意识障碍,IgM水平较术前升高2倍以上,推测可能是术后使用免疫抑制剂导致受者免疫功能下降和弓形虫感染的活化。
肝移植后感染弓形虫的受者多出现播散性弓形虫病,临床表现为脑膜炎、大面积脑水肿和癫痫发作,且常合并巨细胞病毒感染。尽管约70%的肝移植后弓形虫感染受者接受了治疗,但其中仍有40%的受者因弓形虫病而死亡。
上述数据表明,隐性弓形虫感染的活化是肝移植后弓形虫病发病和死亡的主要原因。
1.3 肾移植后的弓形虫病
与心脏移植后的弓形虫病的主要发病机制相似,肾移植后的原发性弓形虫感染主要是由供体感染给受者引起的。
Rogers等报道1例60岁的男性,因节段性肾小球硬化导致的肾衰竭而接受肾移植,移植前受者血清抗弓形虫IgG-、IgM-。在接受抗弓形虫IgG+供体的肾脏移植后第29天,因呼吸困难入院,影像学检查提示该受者患有肺炎,血清学检查显示抗弓形虫IgM-和IgG-,PCR检测从肝、肺组织和血液中检出弓形虫特异性基因。受者于第2天死于心源性休克。尸检组织学观察显示,受者心、肺和肝组织内均存在弓形虫。
另1例59岁女性,因患有终末期肾病而接受了抗弓形虫IgG+供体的肾脏,受者移植前抗弓形虫IgM-和IgG-,在移植后的第28天出现发热、血小板减少等症状,PCR检测血液中弓形虫基因呈阳性,X射线影像学检查显示双侧肺间质浸润,经抗生素(美罗培南)和抗病毒(更昔洛韦)治疗后无好转,出现全身多器官衰竭,转入重症加强护理病房后第4天死于心源性休克。组织学观察发现受者的心、肺和肝等多个脏器组织内存在弓形虫,推测受者的主要死因是播散性弓形虫病。
Segall等报道1例因肾功能衰竭而接受肾移植的受者,受者移植前抗弓形虫抗体阴性,而供体抗弓形虫IgM+、IgG+。在移植后第10天,受者因发热入院,之后出现急性肺水肿、呼吸困难及休克,血清学检测显示抗弓形虫IgM+、IgG+,骨髓活检确诊为弓形虫病。受者于移植后第21天死亡,主要死因是播散性弓形虫病及并发的噬血细胞综合征。
Martina等报道了2例肾移植后弓形虫病病例。1例57岁男性,因肾血管硬化导致终末期肾功能衰竭而接受抗弓形虫IgG+供体的肾移植,受者的巨细胞病毒检查结果阴性、血清抗弓形虫IgG-、IgM-。移植后使用甲氧苄氨嘧啶+磺胺异甲噁唑(TMP+SMX)6个月预防卡氏肺孢子虫感染。但在移植后1年多,受者因发热入院,血清学检查证实为弓形虫原发性感染,无明显临床症状,持续治疗1个月后受者痊愈出院。另1例39岁男性,移植前未做弓形虫血清学检查,在接受D+的肾脏后8个月出现发热,无其他临床症状,血清学检测显示抗弓形虫IgM+、IgG-。给予磺胺类药物治疗后,受者出院时血清抗弓形虫IgM-、IgG+。
对上述病例的分析发现,所有死亡受者均是在移植后的早期(即移植后90d内)出现弓形虫病临床症状,而移植后的晚期(即移植90d后)出现获得性弓形虫病的受者均存活,推测可能与移植晚期受者所使用的免疫抑制药物剂量减小,免疫功能较之前有所恢复有关。
受者移植后晚期弓形虫感染的原因可能是摄入被猫粪污染的水、食物或未煮熟的肉类,经口感染的获得性弓形病发展缓慢、症状较轻并且临床诊断及时,因而移植后晚期获得性弓形虫病受者的存活率较高。
肾移植受者弓形虫病的临床表现多样,发热是最常见的临床症状;其次是肺部不适,弓形虫肺炎的X射线影像学检查常可见肺间质浸润;还可出现弓形虫病神经系统症状如嗜睡、意识混乱、意识改变、癫痫发作和头痛等。少数受者可并发噬血细胞综合征,出现高热、全血细胞减少以及肝功能异常等临床症状,该综合征表现为由单核-巨噬细胞系统被激活,组织巨噬细胞过度增殖并吞噬大量血细胞。虽然噬血细胞综合征在肾移植受者中并不常见,但这种并发症的死亡率极高。
2 SOT后的弓形虫病诊断
器官移植后,有初始弓形虫感染临床表现的受者应尽早诊断,及时的治疗对受者的预后有较大的帮助。然而,在临床实践中SOT受者弓形虫病的诊断仍然很困难,原因是临床表现不典型、受者免疫力低下或应用免疫抑制剂后机体中抗体产生的动力学改变,致使血清学检测的敏感性降低,早期容易漏诊。
2.1 血清学诊断
血清学检测如ELISA、免疫吸附凝集试验和免疫荧光检测等方法是必不可少的手段,器官移植前的血清学检测有助于确定移植前供者和受者血清中抗弓形虫IgM或IgG抗体的滴度、区分原发性弓形虫感染或隐性弓形虫感染的活化。对于D+/R-移植者,若受者移植后早期发生血清学转换,出现抗弓形虫IgM+,则存在从供体获得弓形虫感染的可能。对于D+/R+或D-/R+移植者,若受者移植后出现抗弓形虫IgM+且IgG抗体滴度较移植前升高,则可能是隐性弓形虫感染的活化。免疫抑制剂的大量使用可导致血清学检测的敏感性降低,因而抗体滴度的降低或升高并不能可靠地说明弓形虫病的进展状况。
2.2 PCR诊断
PCR技术可通过扩增B1和AF487550基因来直接识别弓形虫特异性基因,特异性为100%,灵敏度为16%~100%,通过PCR检测血样诊断弓形虫病的敏感性和特异性可分别达80%和98%。
PCR检测近年来已成为诊断SOT受者弓形虫病的主要方法。
PCR技术可检出早期弓形虫感染,对弓形虫感染高风险或不接受药物预防的移植受者应同时进行PCR和血清学检测。有研究者认为,尽管移植后无器官受累的临床表现,但若PCR检测血样呈弓形虫阳性,也可诊断为弓形虫病。因此,对临床上高度怀疑弓形虫感染但血清学无法诊断的器官移植后受者,可优先选择PCR检测血样和其他受感染组织来进行诊断。
2.3 显微镜检查
对组织抽吸物或支气管肺泡灌洗液涂片吉氏染色后,显微镜下查找弓形虫速殖子是诊断弓形虫病简单而快速的方法,也可以对活组织切片进行苏木素或吉氏染色,查找病变脏器中的弓形虫。虽然这些技术快速且价廉,但灵敏度较低。此外,给小鼠接种患者的组织或组织抽吸物也是诊断弓形虫病的有效方法,但需要在接种数周后才能获得明确的结果。
3 SOT后的弓形虫病预防
尽管器官移植前检查供体和受者的血清学抗体可降低移植后受者感染弓形虫的风险,然而目前仅有少数国家对器官捐赠者及移植前的受者进行强制性弓形虫血清学检测,欧洲大部分国家皆是由移植中心决定是否进行血清学筛查。
TMP+SMX可有效地预防弓形虫病,是目前临床上应用最为广泛的药物干预方法。研究表明,给予D+/R-的移植受者6个月以上的TMP+SMX可有效预防弓形虫病。若受者出现磺胺类药物耐受不良,可单独使用乙胺嘧啶作为替代药物,应用乙胺嘧啶可减少SOT受者弓形虫病的发病率。
然而,预防性用药并不能完全消除SOT受者感染弓形虫的风险。有报道显示,在停止使用TMP+SMX预防性治疗后,器官移植受者出现弓形虫病症状,故认为该复合药物虽能有效地延缓弓形虫病的发生,但并不能预防弓形虫病。预防性治疗失败的原因可能是由于药物口服吸收不完全、引起血液毒性以及胃肠道不耐受致使治疗中断所致。
此外,对于移植前和移植后血清学为阴性的低风险受者,应当避免来自环境中弓形虫的感染。
4 SOT后的弓形虫病治疗
目前尚无明确的SOT后的弓形虫病标准化治疗指南,临床上也无治疗的最佳方案,多以乙胺嘧啶加磺胺嘧啶作为首选药物,因为这两种药物对弓形虫有高度的协同作用,通过阻断弓形虫的核酸生物合成通路来抑制速殖子的增殖,对其有快速的杀伤作用。
由于这两种药物均为叶酸抑制剂,可能会引起皮疹、贫血、白细胞减少或肾脏毒性等不良反应,因此临床上辅用叶酸或亚叶酸来预防上述药物引起的严重毒性作用。
另外,大环内酯类抗生素(螺旋霉素、克拉霉素、罗红霉素和阿奇霉素)以及克林霉素也具有一定的抗弓形虫作用。
然而,目前大部分药物仅对杀灭弓形虫速殖子有效,而对组织内的弓形虫包囊无明显效果。
也可通过降低免疫抑制药物的使用剂量使淋巴细胞数量增加,帮助受者恢复免疫功能,避免受者出现弓形虫原发性感染或隐性感染的活化。
5 结语
SOT后的弓形虫病具有较高的发病率和病死率,移植前应对受体和供体进行血清学检查,评估弓形虫病发生的风险。移植前血清中抗弓形虫抗体的状况是SOT受者弓形虫感染的重要影响因素,接受D+移植器官的R-发生弓形虫感染的风险最高。
在SOT受者中,心脏移植受者的弓形虫病发病率最高,而肾脏移植受者在移植后的早期和晚期出现的弓形虫病具有不同的临床结局。
SOT后的弓形虫病临床表现呈多样化和非特异性,可使用PCR检查外周血或受累脏器进行早期诊断,同时可采用血清学检查区分现症感染或既往感染,如果受者被证实患有弓形虫病,应立即给予相应的治疗。
参考文献 略
本文仅供学习参考,完整准确内容请查阅原始文献:黄子芸,吕芳丽.实体器官移植与弓形虫病[J].中国寄生虫学与寄生虫病杂志,2021,39(03):386-392.
【链接】
下一代致命疾病可能来自于家庭宠物
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=31957
|
|