霉酚酸是吗替麦考酚酯(MMF)的水解活性产物,具有较好的免疫抑制作用和较高的安全性,被广泛应用于器官移植,极大提高了受者的生存率。但是霉酚酸血药浓度在不同受者中个体差异大,为更好地控制免疫排斥反应、减少药品不良反应发生,临床推荐药-时曲线下面积(AUC)作为MMF的治疗药物监测(TDM)指标。郑州市第七人民医院回顾性分析229例次受者AUC0-12h监测结果及其临床资料,探讨生理因素对霉酚酸血药浓度的影响,为临床合理使用霉酚酸提供必要依据。现摘录相关内容以供学习参考。
一、一般资料
收集整理郑州市第七人民医院2021全年肾移植科使用MMF并开展霉酚酸血药浓度监测的受者,查阅病历并记录基本资料及联合用药情况。
纳入标准:①首次或者2次肾移植受者,连续服用同一剂量MMF>5d;②在肾移植术前或术中使用抗体诱导治疗;③肾移植术后5年内住院受者,非门诊随访受者;④住院期间多次监测霉酚酸浓度受者,纳入第一次监测数据。
排除标准:①按照Child-Pugh评分,肝脏储备功能B、C级受者;②同时服用含有镁和铝氢氧化物的抗酸剂、考来烯胺等可能影响霉酚酸吸收及肝肠循环的药物者。
最终纳入肾移植科229例住院受者229例次霉酚酸稳态血药浓度监测数据,其中男154例,女75例,年龄(42±11)岁,身体质量指数(22.45±3.82)kg/m2。原发病包括糖尿病肾病46例,慢性肾小球肾炎69例,多囊肾6例,病因不详者108例。
分组:
根据肾移植受者性别分为M组(男)154例和F组(女)75例。
根据肾移植受者体质量分为A组(体质量<50kg)28例、B组(50kg≤体质量<60kg)64例、C组(60kg≤体质量<70kg)62例、D组(70kg≤体质量<80kg)54例和E组(体质量≥80kg)21例。
根据肾移植受者UGT1A8*2基因型分为野生CC型46例、杂合子突变CG型57例和纯合子突变GG型35例。
根据肾移植受者白蛋白水平分为2组,正常组(≥35g/L)202例和低蛋白组(<35g/L)24例。
根据肾移植受者血红蛋白水平可分为3组,分别为正常组(血红蛋白≥120g/L)61例、轻度贫血组(120g/L>血红蛋白≥90g/L)127例、中重度贫血组(90g/L>血红蛋白≥30g/L)34例。
根据肾移植受者的肌酐清除率水平分为4组,分别为正常组(肌酐清除率≥90mL/min)52例、2组(60mL/min≤肌酐清除率<90mL/min)91例、3组(30mL/min≤肌酐清除率<60mL/min)62例和4组(肌酐清除率<30mL/min)21例。
免疫抑制方案:
术后初始抗排斥方案是糖皮质激素+MMF+他克莫司。术后第1天开始口服MMF(每次750mg,q12h),早晚空腹服用。
MMF有2种:MMF分散片,每片0.25g(杭州中美华东制药);MMF胶囊,每粒0.25g(上海罗氏制药)。
二、研究方法
本研究采用的是课题组已建立的全自动二维高效液相色谱测定人血浆中霉酚酸浓度的方法。采用有限取样法估算霉酚酸体内暴露量(AUC0-12h),采集服药前即刻、服药后1、2、4h共4个点血样,参考文献报道公式计算出AUC0-12h。
AUC0-12h=8.217+3.163×C0+0.994×C1+1.334×C2+4.183×C4。
监测霉酚酸AUC0-12h目标范围为30~60μg·h/mL。
三、结果
(一)霉酚酸AUC0-12h分布情况
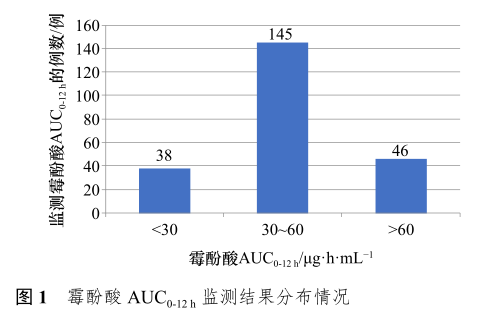
229例霉酚酸AUC0-12h平均值为(45.95±19.25)μg·h/mL,最低值为11.44μg·h/mL,最高值为145.74μg·h/mL。其中有38例AUC0-12h<30μg·h/mL,占总样本量的16.59%;145例在推荐治疗窗(30~60μg·h/mL)之内,占总样本量的63.32%;46例结果>60μg·h/mL,占总样本量的20.09%,见图1。
(二)受者性别差异对霉酚酸AUC0-12h的影响
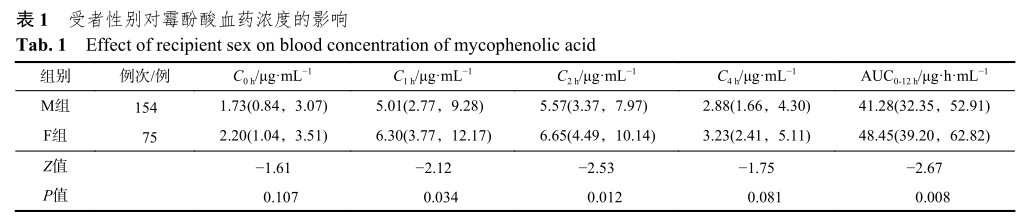
M组(男性)受者霉酚酸AUC0-12h的中位数为41.28,F组(女性)受者霉酚酸AUC0-12h的中位数为48.45,结果显示女性受者的霉酚酸AUC0-12h明显高于男性受者,差异有统计学意义(P=0.008)。同时对不同组别受者的C0h、C1h、C2h、C4h进行比较,C1h、C2hF组大于M组,差异具有统计学意义。结果见表1。
(三)受者体质量对霉酚酸AUC0-12h的影响
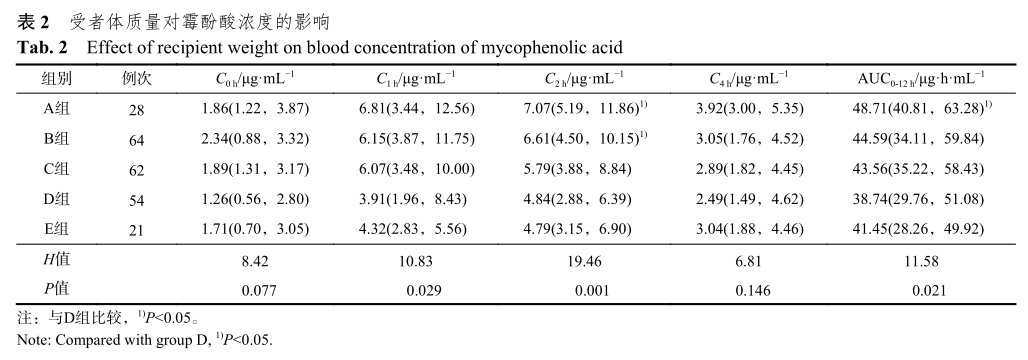
不同体质量的受者霉酚酸AUC0-12h存在明显的统计学差异(H=11.58,P=0.021),D组(体质量≥80kg)与A组(体质量<50kg)
相比霉酚酸AUC0-12h差异有统计学意义(P<0.05)。不同体质量受者霉酚酸AUC0-12h水平呈随体质量的增加而减少的趋势。同时对不同组别受者的C0h、C1h、C2h、C4h进行比较,各组间C0h和C4h无统计学差异,各组间C1h和C2h整体比较有统计学差异且呈随体质量增加而减少的趋势。可见,不同体质量受者霉酚酸AUC0-12h的差异性主要是由C1h和C2h决定的。结果见表2。
(四)尿苷二磷酸葡萄糖醛酸基转移酶(UGT)的一类UGT1A8*2基因多态性对霉酚酸AUC0-12h的影响
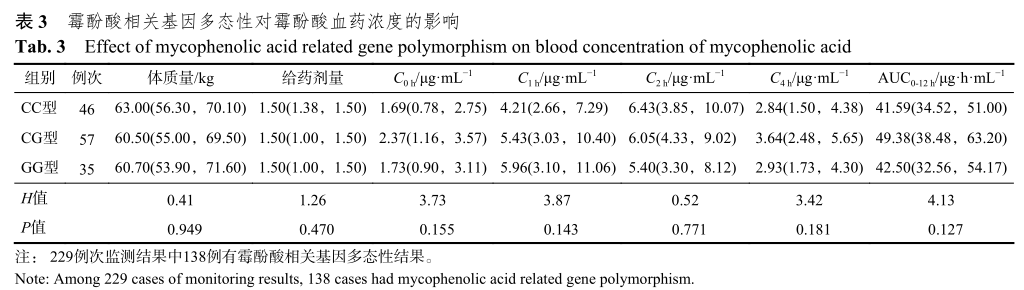
各基因型受者的体质量和给药剂量差异无统计学意义(表3),说明不同基因型组别间受者的体质量和给药剂量无差别。3种基因型组别霉酚酸AUC0-12h值差异无统计学意义。不同组别受者的C0h、C1h、C2h、C4h各组间差异无统计学意义。结果表明,UGT1A8*2基因多态性对霉酚酸AUC0-12h值影响不大。结果见表3。
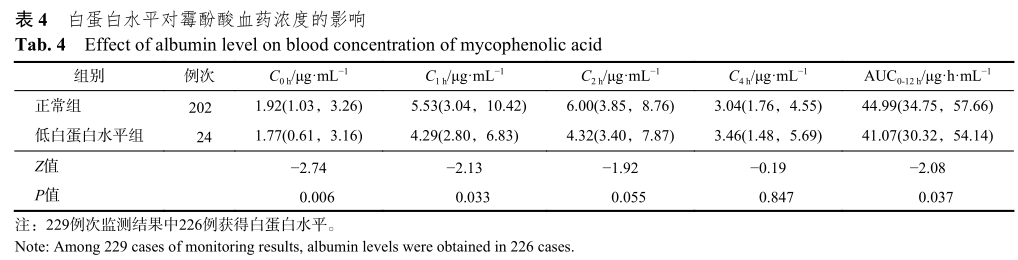
(五)白蛋白水平对霉酚酸AUC0-12h的影响
白蛋白正常水平组的受者霉酚酸AUC0-12h中位数高于低蛋白组,2组间差异有统计学意义(P=0.037)。同时对不同组别受者的C0h、C1h、C2h、C4h进行比较,C0h和C1h差异均具有统计学意义,且均为正常组高于低蛋白水平组,C2h和C4h差异无统计学意义。结果表明正常组的AUC0-12h和C0h、C1h均高于低白蛋白水平组。结果见表4。
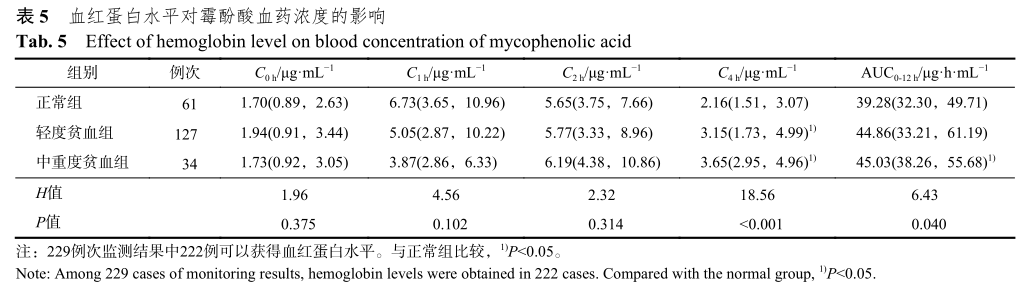
(六)血红蛋白水平对霉酚酸AUC0-12h的影响
不同血红蛋白水平受者霉酚酸AUC0-12h差异有统计学意义(P=0.040)。随着贫血的加重,霉酚酸AUC0-12h有增加趋势。与正常组比较,轻度贫血、中重度贫血组的霉酚酸AUC0-12h中位数均高于正常组,轻度贫血组和正常组相比差异无统计学意义,中重度贫血组和正常组相比差异有统计学意义,说明血红蛋白水平是影响霉酚酸AUC0-12h的因素之一,且呈负相关。同时对不同组别受者的C0h、C1h、C2h、C4h进行比较,C0h、C1h和C2h差异无统计学意义,C4h差异具有统计学意义,但是贫血者C1h是降低的,与贫血者霉酚酸AUC0-12h升高的结果相反,说明血红蛋白对霉酚酸AUC0-12h的影响主要体现在C4h浓度。结果见表5。
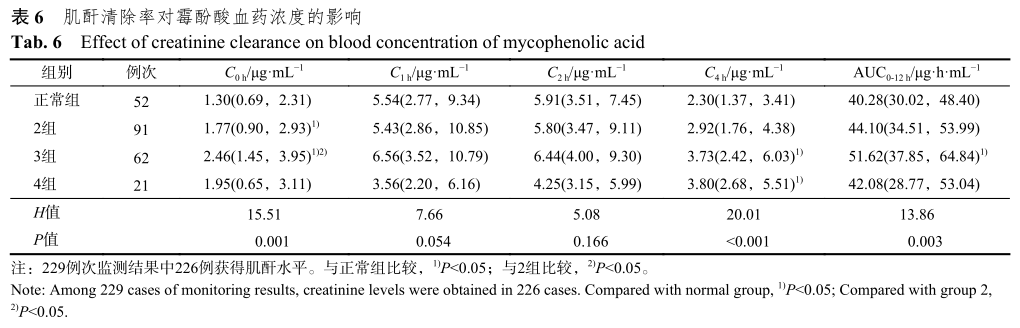
(七)肌酐清除率对霉酚酸AUC0-12h的影响
各组间霉酚酸AUC0-12h差异有统计学意义。2组(60mL/min≤肌酐清除率<90mL/min)和3组(30mL/min≤肌酐清除率<60mL/min)的霉酚酸AUC0-12h中位数均高于正常组(肌酐清除率≥90mL/min),其中,3组与正常组之间的差异有统计学意义。4组(肌酐清除率<30mL/min)与正常组相比未见明显差别,但是此组样本量少,结果可能存在一定的误差。同时对不同组别受者的C0h、C1h、C2h、C4h进行比较,2组、3组的C0h水平均高于正常组且差异具有统计学意义,3组、4组的C4h水平高于正常组且差异有统计学意义。结果表明肌酐清除率较低的受者其霉酚酸AUC0-12h较高,肌酐清除率对霉酚酸AUC0-12h的影响主要体现在C0h和C4h浓度。结果见表6。
四、讨论
本研究229例监测结果中145例在推荐治疗窗(30~60μg·h/mL)之内,占总样本量的63.32%,36.68%未在治疗窗之内,说明监测霉酚酸血药浓度的必要性。
本研究结果表明,受者霉酚酸血药浓度存在性别差异,女性受者的霉酚酸AUC0-12h明显高于男性受者,这一结果也与先前的研究结果相一致。同时,体质量是影响药物体内代谢的因素,文献报道体质量对霉酚酸药动学变化有一定影响。本研究结果表明大体质量受者的霉酚酸暴露量低于小体质量受者,临床上霉酚酸给药剂量整体是按照体质量计算的,给药剂量一般为每天1~1.5g,但是受者体质量差异较大,霉酚酸给药剂量相对固定,故高体质量者霉酚酸暴露量低于低体质量者。女性的体质量一般较男性低,这2项影响因素结果是相符的。那么同时满足以上2个条件,男性受者且大体质量者霉酚酸暴露量较低,而女性受者且小体质量者霉酚酸暴露量较高,故对于男性大体质量者,给予较高剂量以保证移植早期受者霉酚酸血药浓度控制在治疗范围内,对于女性低体质量者,给予较低剂量既能保证药物浓度又可减少不良反应及感染的发生率。临床中使用霉酚酸类药物可以结合性别和体质量适当调整用药剂量,男性大体质量者和女性低体质量者应该个体化给药,并监测霉酚酸血药浓度。
UGTS是体内物质二相转化的一类酶家族,是MMF在体内代谢的重要限速酶,其不同位点的突变会造成包括剂量、血药浓度和不良反应在不同个体间的差异。以往研究报道,UGT1A8*2位点的多态性主要与移植术后MMF所致相关不良反应有关,不良反应的增加可能与增加霉酚酸的暴露量有关,但缺少相关研究。本研究关于UGT1A8*2基因多态性对霉酚酸AUC0-12h的影响进行分析,结果发现不同分型之间霉酚酸AUC0-12h未见显著性差异,但是本研究未纳入基因分型与不良反应、感染发生情况之间的关联,这也是课题组进一步研究的方向。
本研究发现低蛋白水平会降低移植受者霉酚酸AUC0-12h,结果与黄凌斐研究结果相同。血浆中霉酚酸和白蛋白的结合率高达97%,低蛋白状态下,霉酚酸呈游离状态,易代谢排泄,故而霉酚酸血药浓度降低,建议临床对于低蛋白血症者及时纠正低蛋白状态。
血红蛋白水平明显影响霉酚酸AUC0-12h,轻度贫血对霉酚酸AUC0-12h影响不大,中重度贫血受者霉酚酸AUC0-12h显著升高,及时纠正受者贫血状态十分必要。关于血红蛋白对霉酚酸AUC0-12h的影响研究较少,兰州大学王华彬的硕士论文研究结果表明血红蛋白与标准剂量的霉酚酸-AUC呈现较弱但有统计学差异的负相关,这一结果和本研究的结果相符。
肾功能状态显著影响霉酚酸AUC0-12h,肌酐清除率<60mL/min者霉酚酸暴露量显著增加,这可能和霉酚酸主要经肾排泄有关。
综上所述,临床肾移植受者霉酚酸暴露量有显著个体差异,其血药浓度受性别、体质量、血浆白蛋白水平、血红蛋白水平、肾功能等情况影响,建议临床结合生理因素实行个体化给药,特别是受者血浆白蛋白、血红蛋白、肾功能情况出现明显波动时应该加强监测。在使用MMF进行治疗时,给予个体化治疗有利于提高临床治疗效果,提高用药安全性,促进MMF合理用药。本研究是回顾性分析,也有一定的局限性,未来将纳入临床治疗效果和药物不良反应进一步开展前瞻性研究,完善肾移植受者管理方案。
本文仅供学习参考,完整准确内容请查阅原始文献:王长安,韩健乐,杨青彦,索敬钧,杨俊伟,李涛,殷正伟,张寒娟.肾移植受者生理因素对霉酚酸体内暴露量的影响[J].中国现代应用药学,2024,41(22):3167-3173.
【链接】
中国肝、肾移植受者霉酚酸类药物应用专家共识(2023版)(建议要点)
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=89117
药物相互作用对肾移植受者霉酚酸体内暴露量的影响
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=89916
肝肠循环对霉酚酸药动学作用及其影响因素研究进展
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=87640
性别对肾移植受体霉酚酸血药浓度影响的临床分析
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=86950
霉酚酸类药物在器官移植受者中的药代动力学研究进展
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=87380
|