|
|
一些器官移植受者的供者人类白细胞抗原(HLA)分型信息缺失,对其群体反应性抗体(PRA)阳性的可疑抗体介导排斥反应(AMR)患者体内供者特异性抗体(DSA)如何判读?
南方医科大学南方医院器官移植科2022年报道了利用移植肾活检组织对供者进行HLA分型从而判定DSA存在的方法。
一、方法
获取2例可疑AMR患者的新鲜移植肾组织,一部分经消化、提取总DNA后进行供受者HLA分型,将总HLA分型信息与受者外周血HLA分型信息对比,获得供者HLA分型信息。另一部分移植肾组织制作石蜡块,行HE染色、C4d免疫组化等常规病理镜检。结合患者临床表现、病理镜检结果、受者外周血HLA抗体检测结果、供受者HLA分型信息,判断患者是否为DSA介导AMR。
二、病例1
男性,现年48岁,8年前因慢性肾脏病5期于外院接受了1例车祸捐献者供肾,围术期免疫诱导方案为抗人胸腺细胞免疫球蛋白+甲泼尼龙,术后规律服用他克莫司+吗替麦考酚酯+强的松三联抗排斥反应治疗。
2019年因肺部感染至当地医院就诊,停用抗排斥反应药物2月余后发现血清肌酐(Scr)升高,免疫抑制冲击治疗无效并开始规律血液透析,3次/周。
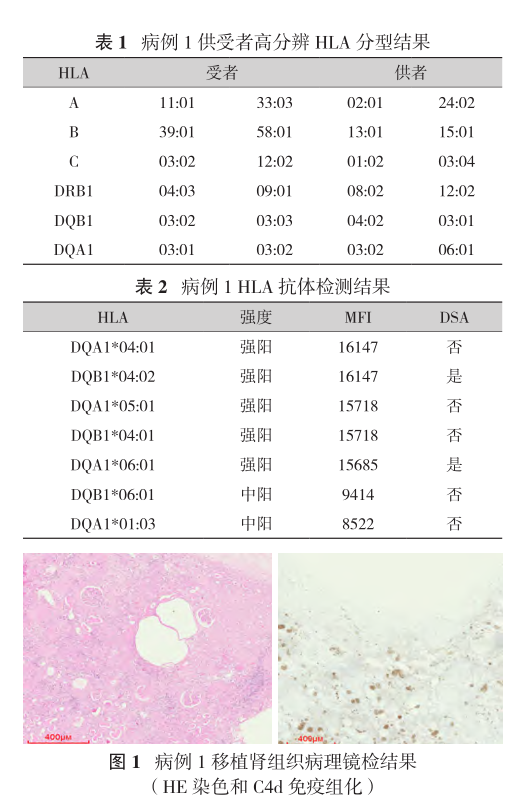
2021年4月,患者诊断为“移植肾功能不全尿毒症期”,欲再次肾移植至南方医院就诊;血清尿素氮(BUN)为37.9mmol/L,Scr为1075μmol/L,尿酸为525μmol/L;移植肾及移植肾血管彩色多普勒检查显示移植肾体积偏小,实质回声增强;CT全腹平扫显示移植肾血管硬化伴移植肾小囊肿;复查PRA(+),遂行移植肾切除术。病理结果显示大部分肾小球萎缩、透明变性、纤维化,肾小管周围血管内皮细胞增生致内膜显著增厚,管腔狭窄闭塞,符合局灶节段性肾小球硬化(FSGS)表现(图1),C4d(-)。
由于供者HLA信息缺失,一部分移植肾组织被用于供受者HLA分型(表1),结合HLA抗体检测结果(表2)拟诊为DSA介导的C4d(-)AMR。术后继续维持血透治疗,目前患者生存情况良好,等待再次移植中。
三、病例2
男性,现年54岁,6年前因慢性肾脏病5期于外院接受了1例脑死亡捐献者供肾。围术期免疫诱导方案为抗人胸腺细胞免疫球蛋白+甲泼尼龙,他克莫司+麦考酚酸+强的松三联抗排斥反应维持治疗。患者术后出现移植肾功能延迟恢复,经血液透析治疗后移植肾功能好转出院,Scr水平维持在130μmol/L左右。
2020年1月患者随诊时尿蛋白(+),予雷公藤多苷治疗,效果欠佳;2021年5月复查尿蛋白(+++),Scr为142μmol/L,尿酸为429μmol/L。移植肾及移植肾血管彩色多普勒检查显示移植肾内各级动脉阻力指数轻度升高,结合爬行肌酐和蛋白尿等,符合移植肾穿刺指征。病理活检结果显示移植肾符合非特殊型FSGS伴中度慢性肾小管-间质损伤,C4d(-)。
由于供者HLA信息缺失,一部分移植肾组织被用于供受者HLA分型(表3),HLA抗体检测结果(表4)显示DSA(-)。予甲泼尼龙冲击治疗3d,复查血肌酐降至125μmol/L,尿蛋白(+),目前患者生存情况良好。

四、讨论
抗体介导排斥反应(AMR)是肾移植术后的一种严重并发症,在1%~10%的肾移植受者中造成近期和长期的移植物损伤。其中,新发供者特异性抗体(DSA)及其持续存在的状态被认为是造成急性或慢性AMR的关键因素。DSA可分为HLA抗体和包括抗ABO、抗次要组织相容性复合物(MiHA)等在内的其他非HLA抗体,其中HLA抗体起主导作用。在肾移植领域,HLA抗体产生的主要原因为供者HLA与受者不相容。在免疫抑制不足的情况下出现新发DSA,多为HLA-Ⅱ类抗体,包括DR、DP和DQ等位点抗体。
群体反应性抗体(PRA)可在一定程度上提示潜在或进展中的AMR,但相较于DSA而言,并不意味着绝对的免疫风险,且肾移植术后PRA阳性群体中DSA阳性患者的移植肾功能和长期存活率远远低于DSA阴性的患者。本组2例患者均在随访过程中丢失供者HLA信息。我院接诊时表现为移植物功能不全、蛋白尿,PRA(+)。病例1、病例2移植肾穿刺病理均显示C4d(-)。结合DSA判读结果可确定病例1存在DSA介导的AMR,患者肌酐维持1000μmol/L以上并大量蛋白尿,遂予以移植物切除;病例2虽有阳性的Ⅱ类HLA抗体,但均不属于DSA,可能由既往输血引起,适当增加免疫抑制后血肌酐显著回落。因此,DSA的判读在AMR的诊断、治疗及预后评估中起到不可替代的作用。
对于拟接受再次移植的患者来说,DSA的判读和首次移植HLA配型相合情况决定了再次移植的供者错配可接受性、再次移植风险评估和术前准备方案。例如,病例1为HLA-Ⅱ类DSA阳性受者,当考虑再次移植时,应当首选HLA-Ⅱ类位点相容率高的供者,其中DQ位点应完全相容;对于HLA-Ⅰ类和Ⅱ类DSA滴度都较高的患者,术后超急性排斥反应风险较大,根据《再次肾移植技术操作规范(2019版)》,予以血浆置换、IVIG应用和利妥昔单抗应用的脱敏预处理。
传统的DSA检测方法基于细胞学的表现,需使用25~60个真实的供者来源淋巴细胞以代表供者的HLA表型分布,然后加入受者的血清检测补体依赖的细胞毒作用。该方法受制于来自于供者的细胞样本,仅适用于移植前的DSA检测,且假阳性、假阴性率均较高。此后问世的酶联免疫吸附技术(ELISA)和随着流式细胞术的发展而产生的基于固相的Luminex分析系统可以高敏感、高通量地测定供者体内Ⅰ类、Ⅱ类HLA抗体,但DSA的判读仍需结合供者的HLA分型信息,尚不能完全满足日益增多的供者HLA分型信息缺失受者的需要。
Liu等从受者中段尿中分离、培养供者来源细胞,提取DNA并对供者HLA基因进行测序与分型。该方法的突出特点为无创与安全,具有很大的应用前景,目前已经实现产学研转化。但由于该方案涉及细胞培养过程,对操作者的实验技术要求较高,耗时较长、较难实现自动化,且费用昂贵,推广仍具有一定难度。
本研究适用于移植肾穿刺组织进行HLA的鉴定,可利用新鲜组织或石蜡切片,虽为有创操作,但用量仅为1立方毫米且无皮髓质的部位要求,对临床症状显著、具有病理活检指征的可疑AMR移植受者并未增加额外的医疗风险。该方法中的组织消化和DNA提取流程简便,较尿沉渣而言,抽提DNA质量更高且稳定,可满足HLA分型需要,最快96h内可报告结果,为临床诊疗争取了更多的时间。虽然该方法无法区分与受者完全相同的供者HLA分型,但该方法的目的本身就是鉴定不相容的HLA位点,因此当DNA含量不足时低分辨HLA分型也能满足临床需求,而高分辨HLA分型技术的应用则会大大降低该情况出现的可能。
综上,本文总结了一种在供者HLA分型信息缺失情况下,利用移植肾活检组织对供者进行HLA分型从而判定DSA存在的方法,为跨地域、跨医疗中心就医的移植肾受者随诊工作提供必要的技术支持。对于可疑AMR患者,应当结合供受者HLA分型、DSA判读与病理活检结果,以作出准确的临床诊断,指导患者的精准治疗。
本文仅供学习参考,完整准确内容请查阅原始文献:黄铭理,王於尘,严紫嫣,方翊灵,刘燕娜,耿舰,邓文锋,肖露露,徐健,苗芸.供者HLA分型信息缺失移植受者DSA判定2例并文献复习[J].实用器官移植电子杂志,2022,10(03):233-236.
【链接】
冯灵斌:肾移植术后群体反应性抗体和供者特异性抗体检查
张明:肾移植术后群体反应性抗体检查
https://bbs.yizhiwang.org.cn/forum.php?mod=viewthread&tid=87335
|
|